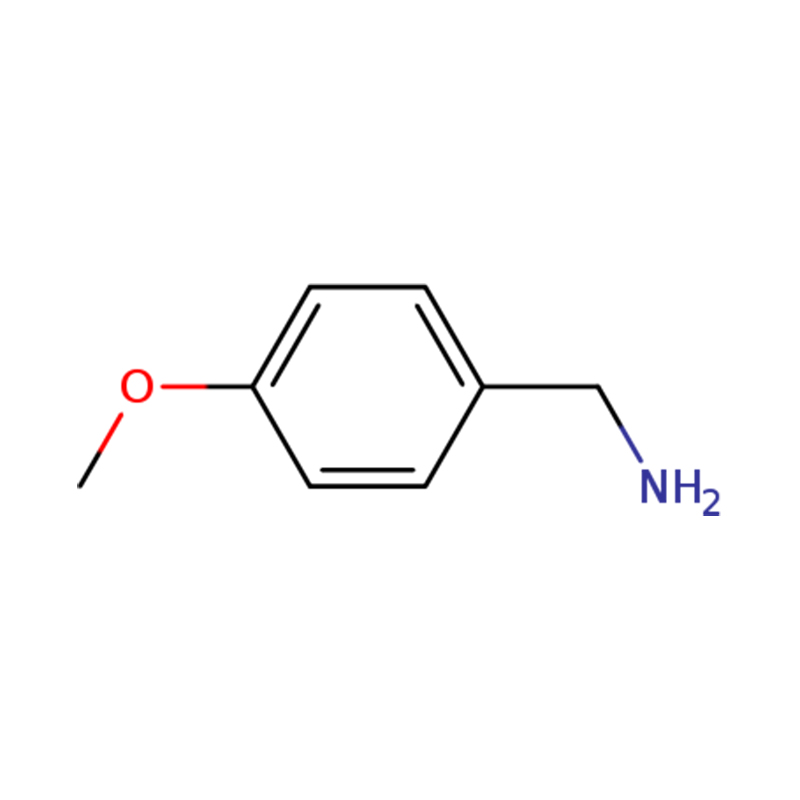
1-(4-მეტოქსიფენილ)მეთანამინი
პროდუქტის დეტალები
| CasNo | 2393-23-9 | მიწოდების დრო | 10 დღის განმავლობაში |
| მოლეკულური | C8H11NO | წარმოების მოცულობა | 1 მეტრული ტონა/დღეში |
| გარეგნობა | გამჭვირვალე, უფეროდან ოდნავ მოყვითალომდე სითხე | სიწმინდე | 99% წთ |
| აპლიკაცია | ფარმაცევტული შუალედური პროდუქტები | შენახვა | ოთახის ტემპერატურაზე, ბნელ, დალუქულ მდგომარეობაში |
| ლიმიტის ნომერი | 1 კილოგრამი | ტრანსპორტირება | საჰაერო, საზღვაო, ექსპრესი. |
| სიმჭიდროვე | 1.05 გ/მ² Lat25°C (ლიტ.) | დუღილის წერტილი | 236-237°C (ლიტ.) |
| დნობის პონიტი | -10°C | რეფრაქციული ინდექსი | n20/D1.546 (ლიტ.) |
| აალების წერტილი: | >230°F | ხსნადობა | წყალში ადვილად ხსნადი |
| სახელი | პ-ანისილამინი ან (4-მეტოქსიფენილ)მეთანამინი |
სინონიმები
LABOTEST-BB LTBB000703; AKOS BBS-00003589; 4-ამინომეთილ-ანისოლი; 4-მეთოქსიბენზილამინი; P-მეთოქსიბენზილამინის ჰიდროქლორიდი 173.64; 4-მეთოქსიბენზილამინი, 98+%; სპარფლოქსაცინისთვის; P-მეთოქსიბენზილამინის ჰიდროქლორიდი
აპლიკაცია
მისი გამოყენება შესაძლებელია ფარმაცევტული შუალედური პროდუქტების სინთეზისთვის. ის ოდნავ საზიანოა წყლისთვის. არ დაუშვათ განუზავებელი ან დიდი რაოდენობით პროდუქტების შეხება მიწისქვეშა წყლებთან, წყლის გზებთან ან კანალიზაციის სისტემებთან. მთავრობის ნებართვის გარეშე, არ ჩაუშვათ მასალები გარემოში, რათა თავიდან აიცილოთ ოქსიდებთან, მჟავებთან, ჰაერთან, ნახშირორჟანგთან კონტაქტი. კონტეინერი ჰერმეტულად დალუქული შეინახეთ, მოათავსეთ ჰერმეტულ გამწოვში და შეინახეთ გრილ, მშრალ ადგილას.
ხარისხის კონტროლის ლაბორატორია
ადგილზე განთავსებულია ინდივიდუალური ხარისხის კონტროლის ლაბორატორია, სადაც ნედლეულისა და მზა პროდუქციისთვის ტარდება ქიმიური, ფიზიკური ტესტირება, მიკრობული ტესტირება, სტაბილურობის შესწავლა და ინსტრუმენტების ტესტირება, როგორიცაა ინფრაწითელი, ულტრაიისფერი, HPLC, GC. მთელი ტერიტორია კონტროლირებადია და კარგად არის მოვლილი, აღჭურვილია საკმარისი ანალიტიკური ინსტრუმენტებით ტესტირების მიზნებისთვის. ყველა ინსტრუმენტი კარგად არის ეტიკეტირებული და შესაბამისად დაკალიბრებული.
QA
ხარისხის უზრუნველყოფის სპეციალისტი პასუხისმგებელია გადახრის შეფასებასა და კატეგორიზაციაზე ძირითად, ზოგად და მცირე დონეებად. გადახრის ყველა დონის შემთხვევაში აუცილებელია გამოძიება ძირითადი ან პოტენციური მიზეზის დასადგენად. გამოძიება უნდა დასრულდეს 7 სამუშაო დღის განმავლობაში. გამოძიების დასრულებისა და ძირითადი მიზეზის იდენტიფიცირების შემდეგ, ასევე საჭიროა პროდუქტის ზემოქმედების შეფასება და CAPA გეგმა. გადახრა იხურება CAPA-ს განხორციელების შემდეგ. ყველა დონის გადახრა უნდა დამტკიცდეს ხარისხის უზრუნველყოფის მენეჯერის მიერ. განხორციელების შემდეგ, CAPA-ს ეფექტურობა დადასტურებულია გეგმის საფუძველზე.